漫长的等待,终于有了回响。
2025年12月7日,驱动基因阴性,PD-L1阳性的非小细胞肺癌患者,最期待的好消息落地了: 依沃西单抗一线治疗PD-L1阳性非小细胞肺癌适应症,正式成功纳入医保!
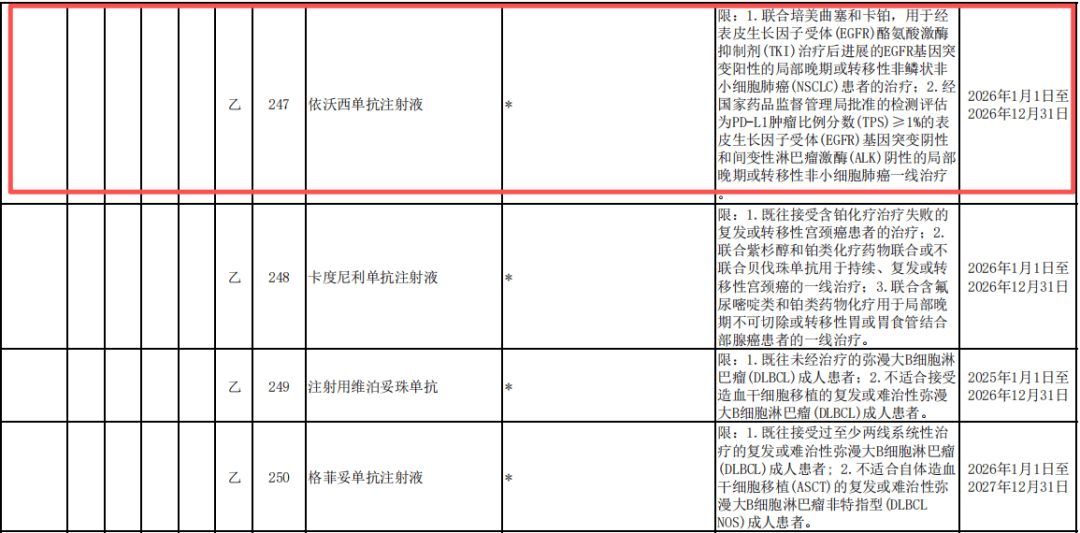
图片来源:国家基本医疗保险、生育保险和工伤保险药品日录(2025年)
01
医保落地:减轻经济负担,治疗方案做减法
根据最新发布的国家医保目录,新版医保将于2026年1月1日正式执行。
【重点:本次医保报销涵盖哪些适应症?】 这次调整后,依沃西单抗在医保内实现了“双覆盖”,无论是初治患者还是耐药患者,都可以报销:
1. 新增适应症(一线治疗):
检测评估为PD-L1肿瘤比例分数(TPS)≥1%的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的局部晚期或转移性非小细胞肺癌一线治疗
划重点:只要PD-L1阳性,没有敏感驱动基因突变,一线单药使用即可报销,不需要联合化疗。
2. 原有适应症(EGFR-TKI 耐药后联合化疗治疗):适用于既往接受EGFR-TKI治疗后疾病进展的局部晚期或转移性非鳞状非小细胞肺癌患者。
划重点:这一项此前已在医保内,本次成功续约,报销范围和治疗方案维持不变。
本次新适应症进入医保后的最终价格,之后会以国家医保局及厂家后续公布的正式文件为准。觅健科普君也在密切关注官方消息,一旦有确切的“第一手价格”和具体报销细则,我们会第一时间在公众号进行更新,请大家保持关注!
医保认可的高性价比,省下的不只是药费
国家医保目录的纳入,不仅仅是价格的博弈,更是对药物经济学价值的官方认证。依沃西单抗此次一线单药的适应症入医保,意味着国家层面认可了其“单药治疗”模式在卫生经济学上优于传统的“化疗+免疫”联合疗法。
减法治疗,降低“直接医疗成本”
传统的联合治疗往往意味着“多药并用”,患者不仅要承担多种药物的费用,还要为化疗及多药联合带来的副作用买单(如处理骨髓抑制的升白针、止吐药、住院费等)。 依沃西单抗的“去化疗”单药方案,从源头上减少了这些因治疗副作用而产生的额外医疗支出。
改善体验,减少家庭“隐形成本”
对于癌症家庭来说,账单不仅在医院。频繁的跑医院、处理复杂的副作用、这就意味着家属需要长期陪护,导致误工和家庭收入减少。 依沃西单抗优异的安全性,让患者体感更好,甚至能回归正常生活。这种对非直接医疗成本(如交通、陪护、误工)的节约,实实在在地减轻了整个患病家庭的负担。
耐受性更佳,保障治疗“连续性”
除了钱,治疗能否坚持下去是更大的挑战。传统化疗带来的剧烈副作用(如恶心呕吐、脱发、极度疲劳),往往是患者产生畏难情绪、甚至被迫中断治疗的主要原因。依沃西单抗单药治疗毒性低、耐受性好,大大降低了患者因副作用而“掉队”的风险,良好的依从性保障了足疗程用药,从而让疗效大打折扣的可能性降到最低。

图片来源:摄图网
提升生活质量,重塑“抗癌信心”
活得久,更要活得好。对于晚期肺癌患者,治疗不应以牺牲生活质量为代价。依沃西单抗在高效控瘤的同时,能让患者相对保持良好的体能和精神状态。这种“像正常人一样生活”的尊严感,能极大增强患者长期抗癌的信心与勇气,帮助患者从心理上完成从“绝症”到“慢病化管理”的积极转变。
真正的好药进医保,就是让患者在获得优异疗效的同时,也能大幅减少治疗的成本。
02
从“无奈之选”到“主动去化疗”,免疫2.0的机制创新带来新希望
依沃西单抗单药进医保之所以备受瞩目,除了经济层面的“减负”,更因为它在临床上走出了一条新路:让PD-L1阳性患者在不依赖化疗的前提下,也能获得优异的疗效。
为了实现这一目标,医学界在平衡“疗效”与“安全性”的道路上,其实经历了一个漫长的探索过程。
最初,免疫单药开启了“希望之门”,但门缝开得不够
PD-1类单靶点抗体药物为代表的免疫单药确实让PD-L1高表达(≥50%)的患者看到了“去化疗”的可能。但对于更广泛的中低表达患者而言,这类单药往往面临“火力不足”的问题,难以完全替代传统方案[1]。
随后,“免疫+化疗”成为主流,疗效提升的同时也带来了挑战
为了解决覆盖面不足的问题,临床上普遍采用了联合治疗模式。确实,免疫联合化疗提升了疗效,但也显露出新的局限:方案复杂难标准化、疗效突破遭遇瓶颈,以及多药叠加带来的毒性管理压力等一系列现实难题。这些问题并不意味着联合治疗“走错了方向”,而是提示我们,疗效和安全性之间的平衡仍需进一步探索[2-4]。
于是,一个新的方向被提出: 如果治疗的“协同”不是靠后天搭配,而是在药物设计之初就植入“协同基因”,是否能打破现有的局限?
依沃西单抗,正是这一“机制协同”理念的最佳实践。
与传统的“你一针我一针”的组合疗法不同,依沃西单抗作为PD-1/VEGF双特异性抗体,不是简单地将两个单抗凑在一起,而是从一开始就以协同为目标进行设计。它通过独特的“四价”结构,在单分子上实现了真正的“一体化协同”:
一手阻断PD-1通路:重新唤醒T细胞的“杀伤力”,负责打破免疫抑制;
一手抑制VEGF通路:阻断肿瘤血管生成,相当于切断癌细胞的“粮草补给”,并改善肿瘤微环境。
这样的设计能让药物真正实现了一场“系统化作战”,从而带来了三重实质性获益:
效率更高:它能“双管齐下”,同时激活免疫系统与改善肿瘤微环境,杀伤力更强、覆盖面更广;
安全性更佳:它是机制上的深度协同,而非简单的药物物理叠加,从而规避了多药联合带来的“毒性累积”风险;
治疗更简化:一支药就能完成两个任务,大大降低了治疗方案的复杂性,让患者的就医体验变得更加轻松、简单。
可以说,依沃西单抗完成了一次对免疫治疗的“系统性重塑”。它证明了:“去化疗”绝非是无奈之下的退而求其次,而是医学科技进阶后的更优选择。这也标志着肺癌免疫治疗正式告别了“拼凑式”组合的1.0时代,进入了精准协同的2.0新阶段。
03
实力说话:HARMONi-2,树立一线治疗新标杆[5]
那么机制上的创新是否真的能转化为临床上的获益?HARMONi-2研究给出了掷地有声的回答
1、PFS达11.14个月,疾病控制率近90%!
在 HARMONi-2 研究中,依沃西单抗单药把中位 PFS 直接拉到 11.14 个月,而对照组的传统免疫单药为5.82 个月;相当于将疾病进展或死亡风险一举压低 49%。同时,客观缓解率从 38.5% 蹿升到 50%,疾病控制率接近 90%,把“更久、更稳”的生存真正落到了看得见的数据上。
目前主流的免疫联合化疗,一线中位 PFS 一般在6-10个月左右,客观缓解率约 40%-60%[3,6-8]。这意味着,依沃西单抗单药的疗效,并没有因为去化疗的关系而减少,反而已与“联合方案”的疗效不相上下。
2、安全性更好:协同设计降低毒性叠加,耐受性更强
与“叠药”带来的毒性不同,根据已公布的临床研究数据来看,依沃西单抗不论是单药使用还是联合化疗,不良反应多为1~2级轻中度(如轻微乏力、皮疹),通过规范的剂量调整、对症治疗(如降压药控制高血压)处理后,基本都能应对。
同时,研究中没有出现新的免疫相关安全信号,有力验证了靶免协同设计避免了常见“毒性叠加”的风险,让患者在治疗过程中少遭罪,生活更有质量。

图片来源:摄图网
3、适用范围广:不挑人群的优选
数据进一步证实,无论是PD-L1低表达患者,还是鳞癌患者,均能从依沃西单抗单药治疗中获得优异疗效,打破了以往单药治疗的局限。
04
中国方案,中国优先:让全球领先的治疗率先惠及国人
依沃西单抗的医保准入,其意义远超一款药物的降价,它代表了中国创新药在“广覆盖”与“高质量”之间的完美平衡。
首先,它填补了临床刚需的缺口。 依沃西单抗医保报销首先覆盖了中国肺癌患者中基数巨大的EGFR突变人群,从我们国家的临床需求出发,为广大EGFR-TKI耐药患者提供有效的治疗手段。
如今,HARMONi-2研究进一步证实,其在更广阔的驱动基因阴性、PD-L1阳性人群(涵盖鳞癌和非鳞癌)中,显著优于现有标准治疗。而医保的 “双覆盖” 更是为患者在关键治疗阶段的用药需求提供了更全面的保障。

图片来源:摄图网
其次,它实现了“好药先给中国人用”。 医保的覆盖会加速这个国际领先的治疗方案优先惠及我国广大肺癌患者。这不仅代表我国创新药水准的提升,更代表国家医保对广大人民医疗保障水平的提高——做到“广覆盖、保基本”,更敢于纳入全球最新的产品,极大地减轻患者负担。
总结
再次划重点,本次医保的变化:
【新增】肺癌一线适应症(2026年1月1日执行):
• 适用人群:用于PD-L1肿瘤比例分数(TPS)≥1%,且无EGFR突变或ALK突变的局部晚期或转移性非小细胞肺癌患者。
• 治疗方案:依沃西单抗单药治疗。
•优势:无需联合化疗,无需驱动基因突变,一线首选即可报销。
【已有】EGFR-TKI治疗进展适应症(已在医保目录内):
• 适用人群:用于既往接受EGFR-TKI治疗后疾病进展的晚期非鳞状非小细胞肺癌患者。
• 治疗方案:依沃西单抗联合化疗(培美曲塞和卡铂)。
未来,相信更多药物进入医保政策,更多患者能在医生的指导下,精准匹配适合自己的治疗方案,在 “用得起、少遭罪、疗效优” 的治疗体验中,收获更长的生存周期与更高的生活质量。医疗进步的意义,从来都是让每一份希望,都能被稳稳接住。
声明:本文内容仅供医学科普参考,具体治疗方案需由专业医生根据患者病情、基因检测结果、肿瘤分期等综合评估后制定。请务必遵循医嘱,切勿自行用药或调整治疗方案。
肺癌
参考文献
[4]Baohui Han, Kai Li, Runxiang Yang, et al. CAMPASS: Benmelstobart in combination with anlotinib vs pembrolizumab in the first-line treatment of advanced non-small cell lung cancer (aNSCLC)—A randomized, single-blind, multicenter phase 3 study. 2025 ASCO Abstract LBA8502.
[5]Xiong, Anwen et al.Ivonescimab versus pembrolizumab for PD-L1-positive non-small cell lung cancer (HARMONi-2): a randomised, double-blind, phase 3 study in China.The Lancet, Volume 405, Issue 10481, 839 - 849
内容制作
封面图片:摄图网





