最近网上流传着“6种常见胃病离胃癌很近”的说法,这其实是一种典型的制造健康焦虑的过度科普。
胃癌的发生确实有一条相对清晰的进阶路径,但并不是所有的“胃不舒服”或者“胃病诊断”都在同一条跑道上,更不是所有胃病“拖久了就会癌变”。简单地把常见的胃病打包在一起吓唬人,既不科学,也没有必要。
我们需要搞清楚的是:哪些才是真正的“癌前”信号?哪些只是需要警惕的误区?
01
从炎症到异型增生
在医学上,真正更接近“胃癌前身”的,通常指的是胃黏膜在长期炎症刺激下出现的结构性改变。这条演变路径通常是这样的:
慢性胃炎 → 萎缩性胃炎 → 肠化生 → 上皮内瘤变(即不典型增生/异型增生) → 胃癌
在这个链条中,“上皮内瘤变”是属于“癌前”概念里最关键的一段。
为了直观地量化不同阶段的风险差异,我们可以参考一项覆盖了9万多名患者的全国队列研究 [1]。研究人员在确诊后进行了长期随访,发现不同诊断人群每年的胃癌发生率有着巨大的鸿沟:
萎缩性胃炎:年发生率为 0.1%;
肠化生:年发生率为 0.25%;
轻中度上皮内瘤变:年发生率为 0.6%;
重度上皮内瘤变:确诊后5年内的年发生率可达 6%。
从下图可以清晰地看到,虽然大家都被称为“胃病”,但风险梯度可以相差几十倍。
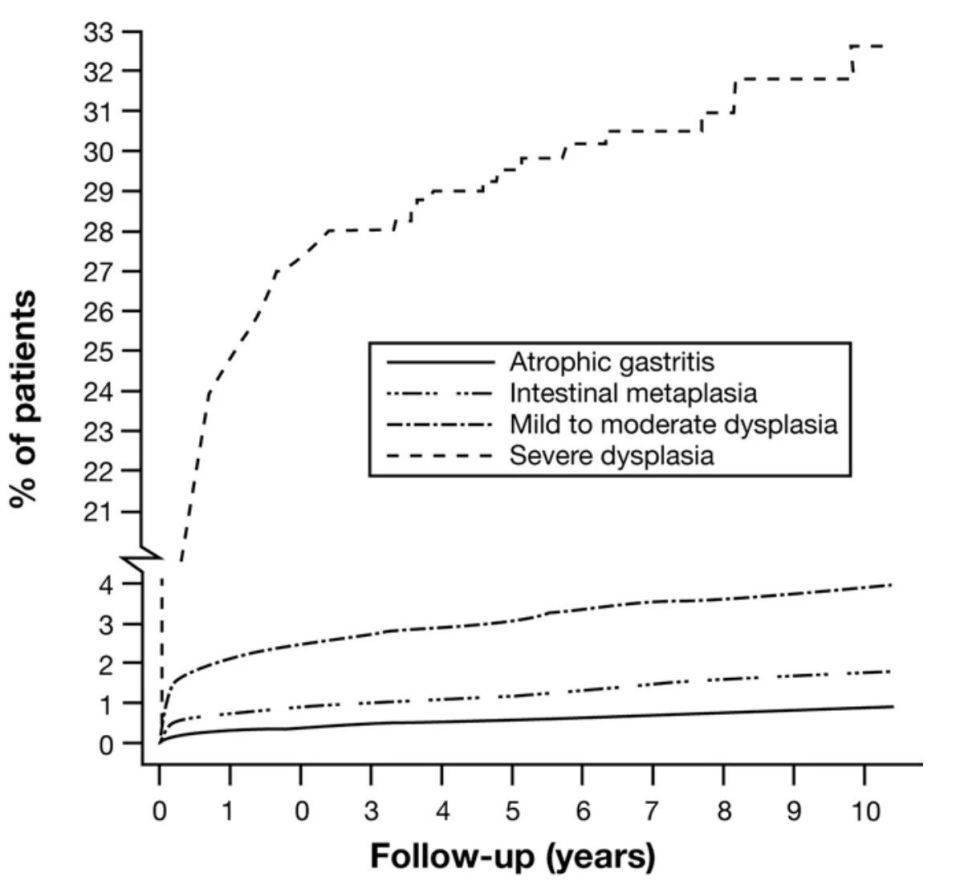
92250例胃癌前病变患者(其中90780例为切除患者)从癌前病变向胃癌的进展率
另一项大样本研究 [2] 则换了一个角度:统计在20年的时间跨度里,大约有多少人最终会发展成胃癌。数据同样说明了问题:
正常黏膜:约 1/256;
单纯胃炎:约 1/85;
萎缩性胃炎:约 1/50;
肠化生:约 1/39;
上皮内瘤变:约 1/19。
这就告诉我们一个很重要的结论:并非所有胃病都会癌变。我们需要对“萎缩、肠化生、上皮内瘤变”这些特定诊断保持严肃态度并定期随访,而不是让所有胃炎患者都被一句“胃病会癌变”吓得睡不着觉。

不同基线诊断患者的胃癌累积发病率
02
最关键干预点:幽门螺杆菌
如果说上面的病变是结果,那么幽门螺杆菌感染就是这条路径里最常见、也最可干预的上游因素。
根据高质量随机试验显示 [3],在有胃癌家族史的高危人群中,根除幽门螺杆菌后,胃癌发生风险比未根除组降低了55%。这是一个非常可观的数字,也是少数能实打实把胃癌风险往下拉的靶点。
建议:当发现幽门螺杆菌感染时,特别是如果您符合以下任一情况,都应该考虑积极、规范地应用药物根除感染:
出现胃肠道症状;
有胃癌家族史;
年龄在40-50岁。
03
不直接等同于癌前病变
再说回那个让很多人焦虑的话题,那里常把胃溃疡、胃食管反流、胃息肉和胃癌强行绑定。事实上,它们的风险含义完全不同。
1. 胃溃疡:重点在于排除而非演变
胃溃疡更准确的定位不是“癌前病变”,而是一种“需要排除癌”的疾病。因为部分胃癌在胃镜下看起来很像溃疡,所以医生要求做活检,是为了确认它到底是不是癌,而不是说所有良性溃疡拖久了都会变成癌。一项队列研究显示,胃溃疡中有 6% 最终被证实为恶性 [4]。这个比例虽然不低,提醒我们要重视活检和复查,但绝大多数胃溃疡依然是良性的,不必因为有了溃疡就觉得是在给癌症倒计时。
2. 胃食管反流:警惕的是食管,而不是胃
胃食管反流病(GERD)主要关联的是食管腺癌的风险,发生的部位是食管,而不是我们通常说的胃体或胃窦部位的胃癌。把它直接描述成“胃癌前身”极易误导方向。对于反流患者,真正需要警惕的信号是:长期反流、吞咽困难、进行性消瘦、呕血黑便等 [5]。出现这些症状需要及时评估,而不是简单把“反酸”等同于“得癌”。
3. 胃息肉:关键看类型
对于胃息肉,不能一概而论,关键在于部分类型有风险。以常见的胃增生性息肉为例,综述数据显示其恶变风险多在 0.6% 到 6.6% 之间,少数研究可达 8.6% [6]。发现息肉后是否需要切除或随访,取决于息肉的具体病理类型、大小、是否合并萎缩/肠化生以及是否有幽门螺杆菌感染等背景。
04
面对胃病,我们该做什么
真正的科普不应该用恐慌来驱动关注,而应该帮大家把风险分层。
查菌杀菌:检查幽门螺杆菌,符合指征的进行规范根除治疗,这是阻断病变源头的关键。
读懂病理:做完胃镜看报告,重点关注“萎缩”、“肠化生”、“上皮内瘤变(异型增生)”这几个关键词。如果有,按医生建议的频率(如一年一次或更频)严格随访。
规范排查:遇到胃溃疡,必须配合医生做规范的活检和治疗后复查,目的是排除那6%混在其中的恶性病变。
关注食管:长期严重的胃食管反流,重点要监测食管的健康状况。
分类处理:胃息肉切不切、怎么管,听医生根据病理类型做的判断,不要自己吓自己。
参考资料:
[1] de Vries AC, et al. Gastric cancer risk in patients with premalignant gastric lesions: a nationwide cohort study in the Netherlands. Gastroenterology. 2008.
[2] Song H, et al. Incidence of gastric cancer among patients with gastric precancerous lesions: observational cohort study in a low risk Western population. BMJ. 2015.
[3] Choi IJ, et al. Family History of Gastric Cancer and Helicobacter pylori Treatment. N Engl J Med. 2020.





