我国肝癌的发病率、死亡率长期处于高位,患者病情特点与西方国家以及日本存在明显差异。多数患者在确诊时,肿瘤负荷已处于中高水平,超70%的患者因病情进展而无法接受手术切除,疾病负担极为沉重。如何突破困境,让更多肝癌患者实现长期生存乃至“无瘤生存”,一直是中国医者不懈探索的方向。
中国肝癌诊疗经历了一条从局部治疗到系统治疗,再到多学科整合治疗的演进之路。近年来,以阿替利珠单抗联合贝伐珠单抗(T+A)为代表的靶向免疫治疗方案,已成为国际国内指南共同推荐的一线标准,显著改善了晚期肝癌患者的生存。然而,中国学者并未止步于此,而是立足本土临床实际需求,进一步思考如何在“控瘤”基础上,为特定患者群体探寻通往“无瘤生存”的可能路径。这种对治疗策略的精细分层与主动突破,催生了一系列具有国际影响力的中国原创研究。2025年相继发布的TALENTACE与TALENTOP研究,正是其中的标志性成果。
TALENTACE研究:奠定联合治疗新范式,实现“1+1>2”的协同突破
TALENTACE研究[1]设计从顶层进行了深刻战略考量(图1)。首先,在研究人群上,TALENTACE研究创新性聚焦“最大肿瘤直径+病灶数量≥6”的中高肿瘤负荷、适合TACE治疗的肝癌患者——这恰恰是我国临床实践中数量庞大、病情复杂严重、治疗需求迫切且单纯依靠传统TACE治疗可能难以达到理想效果的群体。
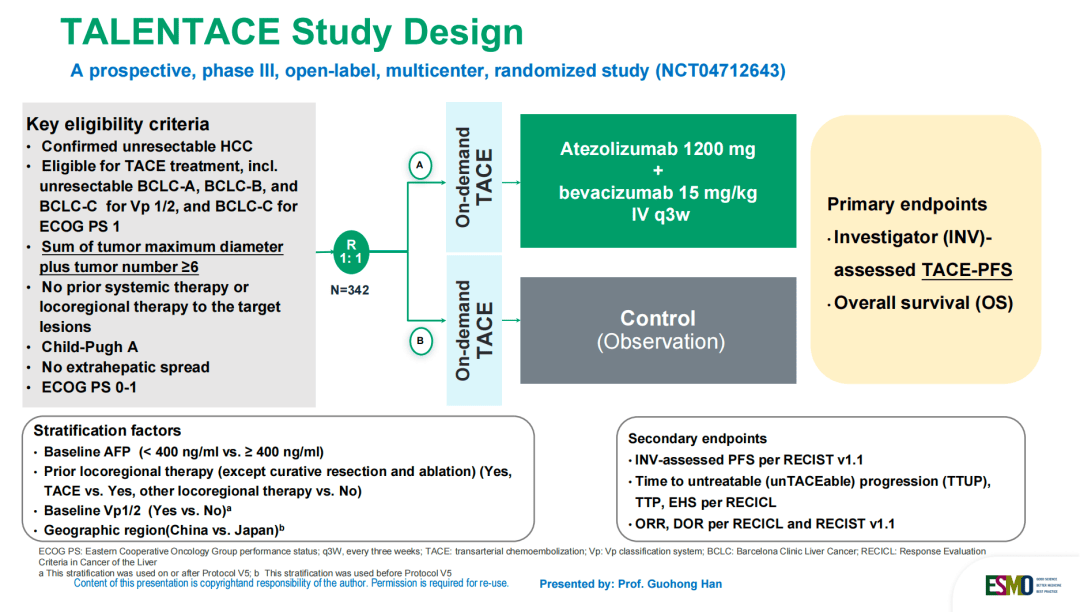
图1. TALENTACE研究设计图
其次,在治疗模式上,TALENTACE研究确立了“按需TACE”联合“T+A系统治疗”的策略:在首次TACE治疗后的2-8周为患者联合使用T+A系统治疗,后续TACE的实施则完全基于影像学评估和患者的整体状况进行个体化决策,不再受固定周期或次数的限制。这种模式高度契合临床实践中根据肿瘤生物学反应进行精准调整的治疗逻辑。
关键数据证实了这一战略的成功:主要终点TACE-PFS(TACE不可治疗进展或TACE抵抗或全因死亡的时间),联合组达到11.30个月,显著优于单纯TACE组的7.03个月(HR=0.71,图2)。此外,根据RECICL标准评估,联合组ORR高达81.3%,CR率达到了39.2%(图3)。这组数据表明,TALENTACE研究的意义,不仅在于有效控制甚至缩小肿瘤,更在于让局部治疗与系统治疗产生真正的“1+1>2”协同突破,将部分传统意义上的“姑息治疗”转化为具有治愈潜能的“转化治疗”。
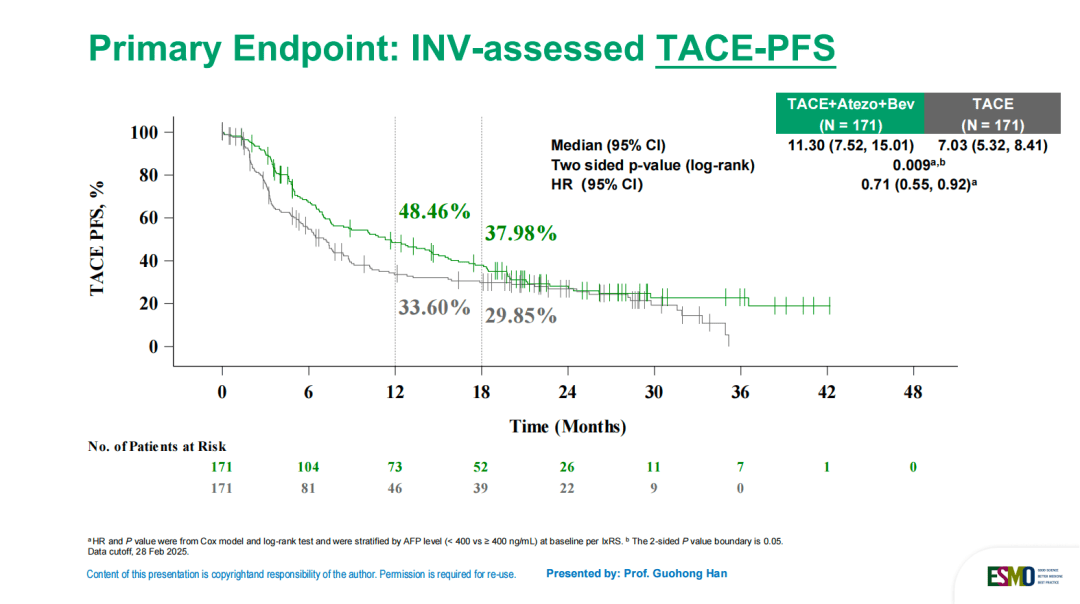
图2. 联合治疗组的中位TACE-PFS显著优于单独TACE组
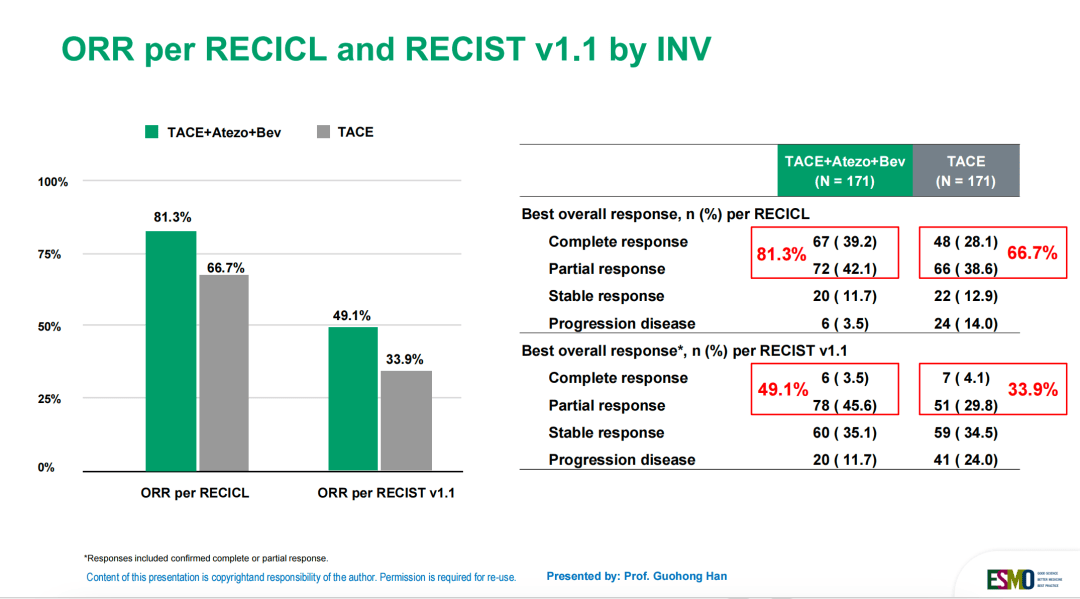
图3. 联合治疗组的ORR较单独TACE组有显著提高
TALENTOP研究:探索从不可切到可切的转化路径,塑造围手术期全程管理模式
医学探索的脚步永不止歇,临床追求的终极目标始终是让患者实现“无瘤生存”。正是在这一目标的指引下,TALENTOP研究[2]应运而生,直接挑战传统治疗边界,探索从控瘤到无瘤的转化路径。
TALENTOP研究精准聚焦国际国内临床诊疗存在争议的伴大血管侵犯CNLC IIIa期患者群体,开创性地设计了“筛选-切除-巩固”完整闭环路径(图4)。所有入组患者首先接受T+A诱导治疗,随后对于达到部分缓解或疾病稳定、且经研究者评估为“技术上可切除”的患者,按照1:1随机划分,分别接受“手术切除+术后T+A辅助治疗”(手术组)和“维持原有T+A治疗”(非手术组)。这一设计直接回答了“对于治疗后实现疾病控制且具备手术切除条件的患者,能否通过‘手术切除+术后辅助治疗’策略进一步最大化根治可能性”这一核心问题。
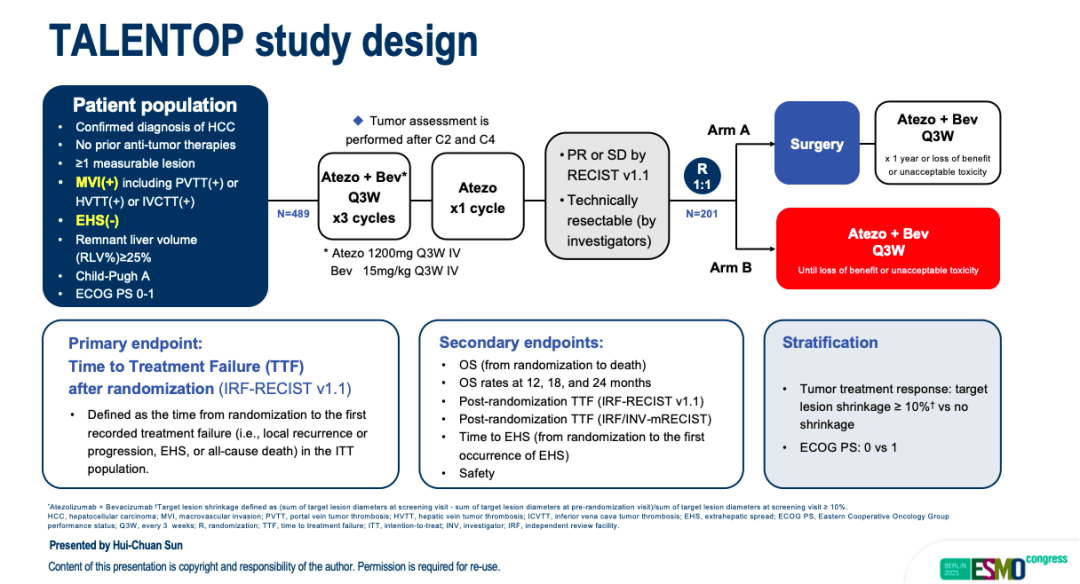
图4. TALENTOP研究设计图
研究结果给出了明确的答案:主要终点TTF(至治疗失败时间)长达20.4个月,相比非手术组的11.8个月实现了接近翻倍的延长(HR=0.60,图5)。亚组分析进一步提示,在肝静脉侵犯和Vp3型门静脉癌栓这两个传统预后极差的亚组中,HR分别达到了0.32和0.46,提示这些传统上最棘手的患者,恰恰可能是从这种积极手术策略中获益最大的人群。 这项中国答案,有力地推动了晚期肝癌治疗从“以疾病控制为中心”的慢病化管理模式,向“以无瘤治愈为目标”的积极干预模式的战略转变,成为全球转化治疗的里程碑。
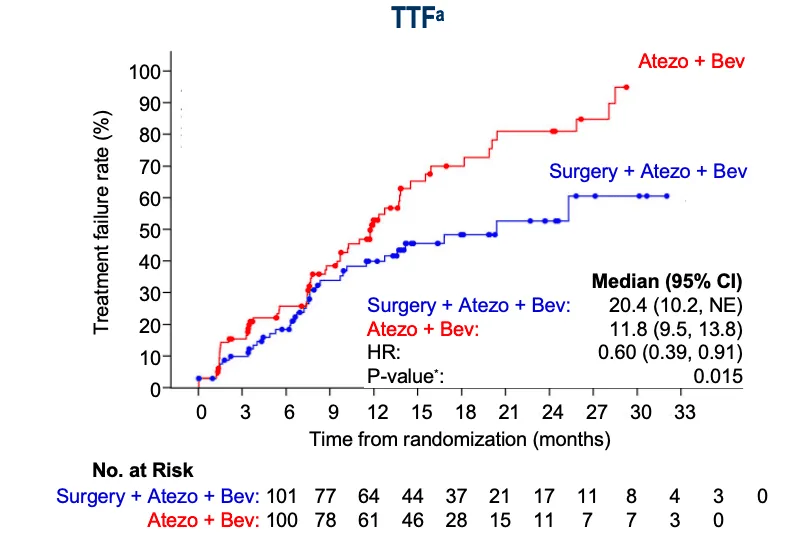
图5. ITT分析显示手术组的TTF(IRF-RECIST v1.1)显著优于非手术组
TALENTACE和TALENTOP两项研究取得阳性结果的价值,不仅在于提供了更新更优的治疗方案,让中国肝癌患者在“控瘤-无瘤”这一征途上迈进一大步,更在于构建了符合中国国情、整合多学科优势的诊疗新范式,向全球专家力证中国肝癌领域完全有能力开展同类首创的临床研究,为全球肝癌诊疗贡献中国智慧。
展望未来,我们相信,将会有更多以TALENTACE和TALENTOP为起点的中国原创“TALENT”系列研究涌现,为中国乃至全球肝癌患者,搏一个“无瘤生存”的机会!





