胃黏液腺癌(Gastric mucinous adenocarcinoma,GMC)是胃癌的罕见亚型,特征为黏液过度分泌、生物学行为侵袭性强、预后较差,多数患者初诊时已处于转移性疾病阶段,失去根治性切除的机会。目前,转化治疗场景下的转移性胃黏液腺癌尚无标准化诊疗指南,常规化疗的治疗效果仍不理想。本文报告 1 例 69 岁男性患者,确诊为HER2阴性、肿瘤突变负荷高(TMB-H)的晚期胃黏液腺癌,伴腹腔及腹膜后淋巴结转移。多学科团队(MDT)最初评估认为该患者肿瘤不可切除,但由于患者治疗意愿强烈且体力状态良好(美国东部肿瘤协作组体力状态评分ECOG-PS=0),选择接受转化治疗。患者接受了 6 个周期的FLOT化疗联合纳武利尤单抗治疗,根据实体瘤疗效评价标准1.1版(RECIST 1.1)评估达到部分缓解(PR)。随后行腹腔镜下远端胃次全切除术(D2+淋巴结清扫术),术后病理显示接近病理完全缓解(Mandard肿瘤退缩分级1级,Mandard-TRG1),无淋巴结转移(0/21),病理分期为ypTisN0。术后患者接受 4 个周期的XELOX化疗联合纳武利尤单抗治疗,后续接受卡培他滨联合纳武利尤单抗同步巩固放疗,之后继续采用卡培他滨联合纳武利尤单抗维持治疗,直至 2023 年 1 月确认持续无疾病证据(NED)。定期随访监测(包括 2025 年 5 月最新的增强CT检查)显示无复发或转移,无进展生存期(PFS)已超过 5 年。这种优异且持续的治疗应答可能归因于TMB-H与DNA聚合酶δ1(POLD1)突变的协同效应,二者可促进新生抗原生成,提升肿瘤对免疫治疗的敏感性。本病例凸显了生物标志物指导下的化疗-免疫治疗联合多学科团队引导的多模式治疗(手术+辅助治疗+巩固放疗),有望为转移性胃黏液腺癌患者实现治愈目标,为这一预后不良人群的个体化治疗策略提供了宝贵参考。
背 景
胃癌(Gastric cancer,GC)是全球发病率排名第五的恶性肿瘤,也是癌症相关死亡的第三大诱因,对人类健康构成严重威胁。黏液腺癌是起源于上皮组织的恶性肿瘤亚型,特征为黏液过度分泌;组织学表现为癌细胞内或细胞外存在大量黏液蓄积,该类癌主要好发于胃与肠道。过去十年间,靶向治疗的显著获益仅局限于接受曲妥珠单抗联合化疗的HER2阳性患者。对于HER2阴性的转移性胃癌患者,全身化疗历来被视为一线治疗方案,但该方案的中位总生存期(Overall Survival,OS)不足 1 年。
随着免疫检查点抑制剂(Immune Checkpoint Inhibitors,ICIs)的发展,免疫治疗已取得可观成效,显著改善了胃癌患者的预后。一系列关键性临床试验推动了不同疾病分期胃癌免疫治疗的格局革新。全球III期研究CheckMate-649证实,纳武利尤单抗联合化疗可显著改善晚期胃癌/胃食管结合部(Gastroesophageal Junction,GEJ)癌一线治疗的长期生存情况,其中中国亚组数据显示,PD-L1 联合阳性评分(Combined Positive Score,CPS)≥5 的患者 4 年总生存期(OS)率达25%,全人群4年OS率达21%,远高于单纯化疗组。ORIENT-16研究证实,信迪利单抗联合化疗可将PD-L1 CPS≥5的晚期胃癌/胃食管结合部腺癌患者的中位OS延长至 19.2 个月(对照组为 12.9 个月),全部随机入组人群的中位OS延长至 15.2 个月(对照组为 12.3 个月),3 年OS率是化疗组的2倍,且安全性可控。全球III期试验RATIONALE-305显示,替雷利珠单抗联合化疗可将HER2阴性晚期胃癌/胃食管结合部癌意向治疗人群的中位OS提升至15.0个月(对照组为 12.9 个月),PD-L1 肿瘤面积阳性(Tumor Area Positive, TAP)≥5% 的患者中位OS提升至16.4个月(对照组为 12.8 个月),死亡风险降低 20%-29%。
针对可切除疾病,MATTERHORN研究证实,围手术期度伐利尤单抗联合FLOT化疗可将疾病进展、复发或死亡风险降低 29%,2 年无事件生存期(Event-Free Survival, EFS)率达 67.4%(单纯化疗组为 58.5%),且OS呈现获益趋势;DANTE试验发现,围手术期FLOT方案基础上加用阿替利珠单抗可提升病理降期率与病理完全缓解(pathological Complete Response,pCR)率(24% vs 15%),在微卫星不稳定(Microsatellite Instability,MSI)或PD-L1 CPS≥10亚组中获益尤为突出,安全性与化疗相当;II期试验NEOSUMMIT-01显示,特瑞普利单抗联合SOX/XELOX化疗治疗局部进展期胃癌,可获得显著更高的主要病理缓解率(44.4% vs 20.4%)与pCR率(22.2% vs 7.4%),错配修复缺陷(Mismatch Repair Deficient,dMMR)患者获益尤为显著,且未增加围手术期安全风险。
尽管如此,仍有相当比例的胃癌患者对ICIs治疗不敏感,这仍是晚期胃癌免疫治疗领域现存的挑战。本文报告 1 例HER2阴性、高肿瘤突变负荷(TMB-H)伴POLD1突变的转移性胃癌患者,接受化疗联合免疫治疗(纳武利尤单抗)的转化治疗后无进展生存期(PFS)超过 5 年。本文同时综述了相关文献,探讨TMB-H与POLD1突变对胃癌免疫治疗应答的潜在预测价值。
病 例
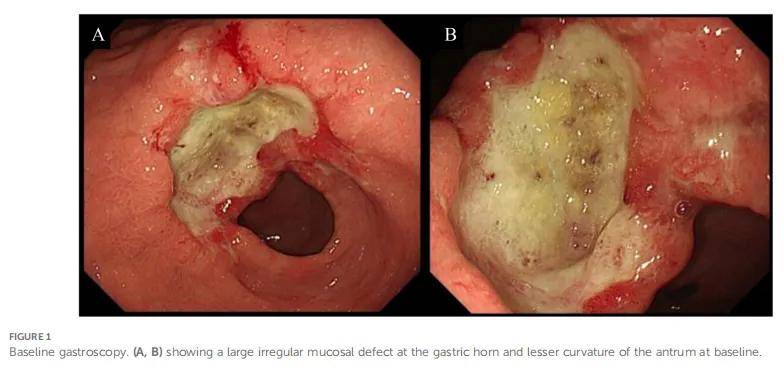
患者男,69 岁,因上腹胀不适 7 月余、近 2 周症状加重,于 2020 年 12 月 7 日收治入院。患者既往史、家族史、心理社会史及相关合并症均无特殊。入院查体未见异常,实验室检查无贫血或感染征象,但肿瘤标志物糖类抗原72-4(CA72-4)水平升高,达 77.16 U/mL(正常值 <7 U/mL)。胃镜检查(2020 年 11 月 26 日,图1)显示:胃角、胃窦小弯侧可见一巨大深在不规则溃疡,边界清晰;周边黏膜呈不规则结节状隆起,表面溃疡坏死明显,覆厚苔,活检组织质脆易出血;胃窦腔狭窄,胃角及胃窦蠕动差。病理分析诊断为胃窦低分化黏液腺癌,Lauren分型为弥漫型。后续免疫组化(图2)提示错配修复功能完整(pMMR),PD-L1阳性(CPS=1)。分子检测证实EB病毒编码小RNA(EBER)、HER2均为阴性。

▲图1 基线胃镜检查
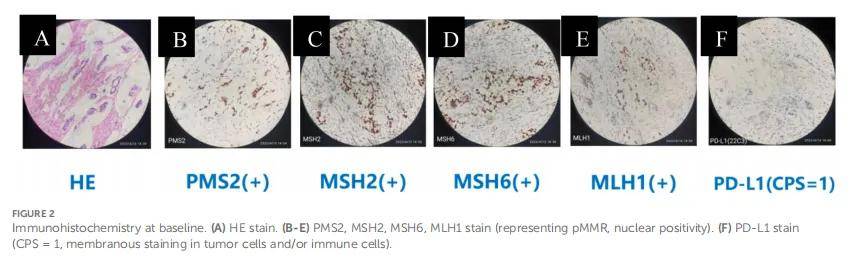
▲图2 基线免疫组化
腹部动态增强CT(图3)显示胃窦壁增厚,穿透浆膜下结缔组织,第3-9组、12-14组淋巴结多发肿大;其中第7、8、9、12、13组肿大淋巴结形成巨大II区淋巴结并包绕门静脉,考虑为转移灶。为更好地指导治疗,研究人员安排患者接受二代测序(NGS)检测,结果提示为高肿瘤突变负荷(TMB-H):85.7 个突变/兆碱基,突变负荷位于人群前 3.1%,同时存在POLD1基因第24号外显子p.R1009H错义突变。

▲图3 基线增强腹部CT复查
患者确诊为转移性胃黏液腺癌,根据美国癌症联合委员会(AJCC)第8版分期为cT3N3aM1、IVB期,伴腹腔及腹膜后淋巴结转移。多学科团队(MDT)评估认为,由于淋巴结受累范围广泛,尤其是第 16 组淋巴结被包绕,初诊时肿瘤不可切除。结合患者强烈的治疗意愿及当前良好的身体状态(美国东部肿瘤协作组体力状态评分[ECOG-PS]=0),推荐采用化疗联合免疫治疗的转化治疗方案,目标为使肿瘤降期,从而有望接受根治性切除,达到无疾病证据(NED)状态。2020 年 12 月 16 日至 2021 年 3 月 11 日期间,患者接受 6 个周期的FLOT方案化疗联合免疫治疗的转化治疗,具体给药方案为:白蛋白紫杉醇 170 mg、奥沙利铂 150 mg、左亚叶酸钙 180 mg、氟尿嘧啶 4.75 g持续静脉输注 46 小时,每 2 周给药1次;纳武利尤单抗 300 mg,每 3 周给药 1 次。患者耐受良好,仅出现I级恶心、II级粒细胞减少,同时上腹胀症状缓解,无体重下降。4 个周期治疗后(治疗中期)的再分期CT扫描及MDT复核显示,患者达到显著部分缓解(PR,参照实体瘤疗效评价标准1.1版[RECIST 1.1]),胃原发肿瘤及转移性淋巴结均明显缩小,但肝门区(第 12/13 组)仍残留巨大淋巴结,与门静脉血管相邻的边界不清,当时无法安全开展手术切除。MDT建议完成原定的 6 个周期化学免疫治疗。6 个周期治疗后的再分期CT(图4)显示,与 4 个周期后的扫描结果相比疾病稳定,无进一步明显退缩。鉴于初始应答优异、疾病已稳定,且残留病灶经评估具备潜在可切除性,MDT与患者共同选择行手术干预,后续针对腹膜后淋巴结引流区行辅助放疗,以巩固治疗应答、达到NED状态。
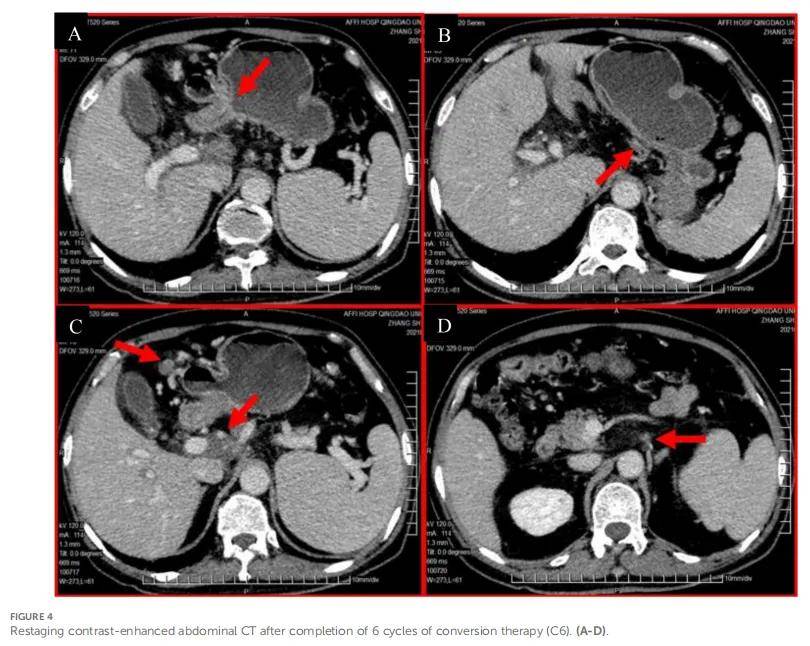
▲图4 完成6个疗程的转化治疗后进行增强腹部CT复查
患者于 2021 年 4 月 1 日行腹腔镜姑息性远端胃次全切除术(D2+,毕II式+Braun吻合)。术中腹腔镜探查结果:无腹水,肝脏外观正常,无表面结节,无可见腹膜种植灶;但肿瘤位于胃角及胃窦小弯侧,累及浆膜。术中操作过程:将大网膜提起使其紧贴横结肠,使用超声刀切开胃结肠韧带,向左游离至结肠脾曲;在胰腺表面解剖分离胃网膜左血管,离断血管后行第4sb组淋巴结清扫,随后继续向上游离胃大弯。将胃结肠韧带向右游离至结肠肝曲,将大网膜向上腹部牵拉暴露胰腺下缘,确认融合间隙后继续向右游离暴露胰头,随后解剖离断胃网膜右动静脉,行第6组淋巴结清扫。在幽门远端 2 cm处使用腔镜下直线切割吻合器离断十二指肠球部;解剖暴露肝总动脉,观察到第8、12组肿大淋巴结已包绕门静脉,且与肝门部浸润固定,无法手术切除,在病灶部位放置银夹,便于后续放疗精准定位。随后在胃右动脉起始部结扎离断胃右血管,将胃向上牵拉暴露胰腺上缘,解剖游离胃左动脉及脾动脉,行第7、9、11p组淋巴结清扫;之后结扎离断冠状静脉及胃左血管,将全胃整块向腹部左上象限牵拉,结扎离断肝胃韧带以游离胃小弯,进一步向上游离至贲门右侧,完成第1、3组淋巴结清扫。手术过程顺利。术后病理提示:慢性中度炎症伴溃疡形成(大小 2.5×2 cm),局灶腺体呈高级别上皮内瘤变;黏膜内癌形态可见细胞嗜酸性变性,周围为增生的间质纤维组织,伴大量淋巴细胞、浆细胞及部分中性粒细胞浸润,符合化疗后改变。肿瘤退缩分级(Mandard-TRG)为 1 级(接近完全退缩,残留肿瘤占病灶面积 <10%)。胃小弯侧(0/13)及胃大弯侧(0/8)淋巴结均未见转移。病理分期:ypTis(黏膜内原位癌,提示治疗后残留病灶)ypN0(0/21),参照AJCC第8版分期标准(图5)。
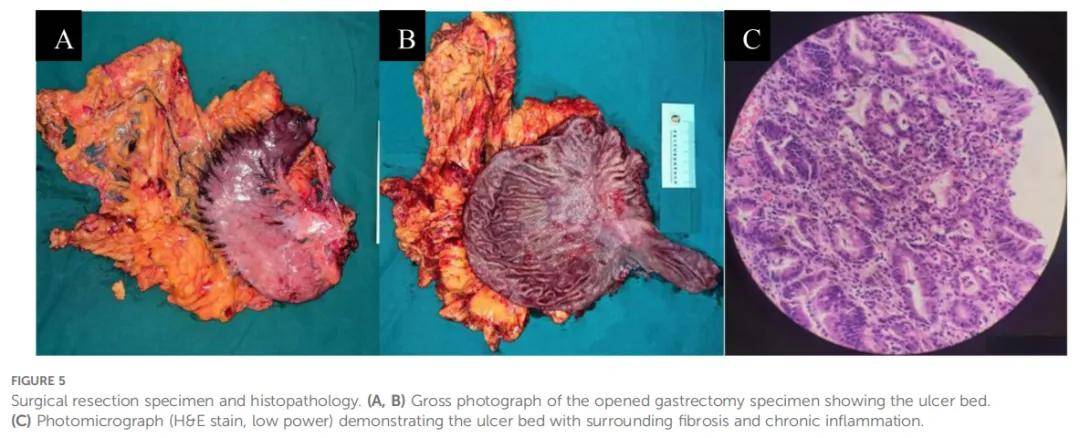
▲图5 手术切除标本及组织病理学检查
术后患者出现胃排空延迟(残胃潴留)及乏力症状。经科室讨论后,将治疗方案调整为 4 个周期XELOX方案化疗(奥沙利铂 125 mg 第 1 天给药+卡培他滨 1.5g 每日 2 次,第 1-10 天给药,每 2 周为 1 周期),联合纳武利尤单抗免疫治疗(300 mg 静脉输注,每 3 周 1 次)。7 月 15 日再分期CT未见复发或转移征象,提示治疗持续缓解(部分缓解,PR)。随后于 2021 年 8 月 4 日至 9 月 7 日对高危淋巴结区域(肝门区、腹腔干周围、腹膜后)实施巩固放疗(图6),同步给予卡培他滨(放疗日按 825 mg/m²剂量每日 2 次给药)及纳武利尤单抗治疗。放疗处方剂量为:受累淋巴结计划大体肿瘤靶区(PGTV)54 Gy,分 25 次照射;淋巴结预防照射计划靶区(PTV)45 Gy,分 25 次照射(二者单次分割剂量分别为 2.16 Gy、1.8 Gy,每周照射 5 次)。患者对治疗耐受良好,仅出现I级胃肠道不良反应。
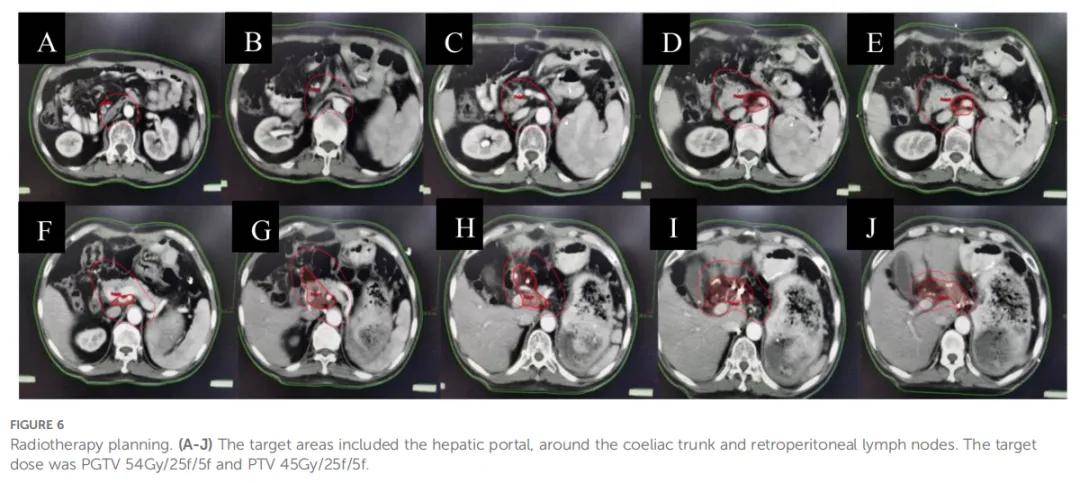
▲图6 放疗计划
患者继续接受卡培他滨联合纳武利尤单抗维持治疗,连续的胸腹部随访CT扫描确认缓解状态持续。2023 年 1 月CT扫描证实达到无疾病证据(NED)状态,因此停止维持治疗。后续定期检查(包括最新的 2024 年 5 月、11 月及 2025 年 5 月CT扫描,图7)仍未显示复发征象,患者目前健康状态良好,无进展生存期已超过 5 年,治疗时间线总结见图8。
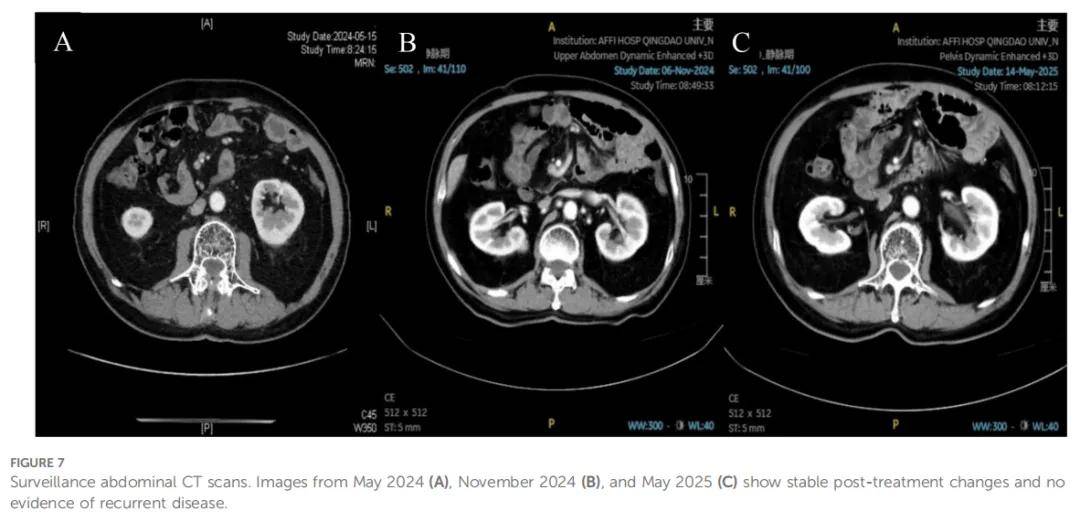
▲图7 腹部CT扫描随访

▲图8 治疗时间线
讨 论
本例初诊不可切除的转移性胃癌患者所取得的优异且持久的治疗应答,可归因于多因素的协同作用:基于生物标志物的严谨患者筛选、有效的多模式治疗,以及体系化的多学科团队(MDT)诊疗模式。
基于生物标志物的患者选择:TMB和POLD1的作用
化疗联合免疫治疗方案的推荐,主要基于 2020 年欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)大会公布的CheckMate-649研究结果,该研究证实免疫治疗联合化疗可显著提升晚期胃癌或胃食管结合部腺癌患者的客观缓解率与生存结局。尽管该联合方案的推荐并非基于TMB-H状态,但本例患者的超高肿瘤突变负荷(TMB= 85.7 个突变/兆碱基)及POLD1 p.R1009H突变的存在,是理解其对免疫治疗产生深度应答的核心因素。TMB可作为新抗原负荷的替代标志物,能够增强免疫识别与T细胞活化。POLD1编码DNA聚合酶δ的催化亚基,是参与DNA复制与修复的关键酶。已知的致癌性POLD1突变包括E245K、E318K、D402N、L474P、S478N、L606M、L632M、R689W及R1016H。尽管目前POLD1 p.R1009H变异被归类为意义未明变异(Variant of Uncertain Significance,VUS),但其位于对DNA校对功能至关重要的核酸外切酶结构域内,强烈提示其具备功能意义。已知该结构域的缺陷会降低复制保真度,加速突变发生,促进超突变表型形成。一项特瑞普利单抗的II期临床试验显示,抗PD-1治疗在POLE/POLD1核酸外切酶结构域突变的肿瘤中可带来优异的客观缓解率(66.7%)。该突变与极高TMB共存的特征,支持了二者的协同作用机制:DNA修复缺陷会放大新抗原生成,从而使肿瘤微环境处于预激活状态,提升免疫检查点抑制剂(ICIs)应答率。
近期的单细胞RNA测序(single-cell RNA sequencing,scRNA-seq)研究为免疫治疗过程中肿瘤免疫微环境的动态变化提供了前所未有的洞见。Huang等人利用scRNA-seq绘制了接受ICIs治疗的癌症患者的免疫细胞组成及功能状态图谱,发现TMB-H肿瘤的特征是具备独特的免疫微环境,其中富集了克隆扩增的效应CD8+ T细胞、活化树突状细胞,且髓源性抑制细胞(Myeloid-Derived Suppressor Cells,MDSCs)含量更低。本例患者尽管PD-L1 CPS=1,处于相对较低的水平,但超高TMB(85.7个突变/兆碱基)很可能将免疫微环境重塑为“炎症”表型——这与该研究中“基因超突变与T细胞浸润及功能活化增强相关”的结论一致。该scRNA-seq来源的证据进一步验证了我们的假设:即使在PD-L1低表达的转移性胃癌中,TMB-H与POLD1突变共存也可赋予肿瘤极高的ICI敏感性。
Pauken等人阐述的新辅助ICI治疗的基础免疫学机制,进一步支持了我们转化治疗策略的有效性。他们的研究证实,新辅助免疫治疗可诱导全身T细胞启动及克隆扩增,新抗原特异性T细胞可长期持续存在以预防复发——这一效应在新高抗原负荷肿瘤(如TMB-H肿瘤)中尤为显著。本例患者中,转化化学免疫治疗不仅实现了显著的部分缓解,还诱导了持久的免疫记忆应答,超过5年的无进展生存期便是佐证。这与Pauken等人的结论一致:基于ICI的新辅助/转化治疗方案可通过靶向既存新抗原,充分释放抗肿瘤免疫的潜力,这一点对超突变肿瘤尤其适用。
He等人开展的一项前瞻性研究为POLD1突变在胃癌免疫治疗中的预后及预测价值提供了直接证据,该研究分析了接受ICI治疗的HER2阴性晚期胃癌患者的循环肿瘤DNA(circulating Tumor DNA,ctDNA)。研究结果显示,与不存在这类共突变的患者相比,携带POLD1相关共突变(如IRS2/POLD1或POLD1/CEBPA)的患者中位PFS显著延长(p值分别为 0.006 和 0.0315)。值得注意的是,该研究强调,POLD1突变可通过加剧基因组不稳定性、增加新抗原呈递,独立提升ICI应答率。
近期的泛癌分析进一步支持了这一论断,研究显示,与野生型患者相比,携带POLE/POLD1突变的患者接受ICI治疗后的生存期显著延长。具体到消化道肿瘤中,携带这类突变的患者中位总生存期为 34 个月,而无突变的患者仅为 18 个月。这些极具说服力的临床证据进一步印证了:即使特定变异的功能尚未明确,POLD1驱动的超突变可作为免疫治疗疗效的预测生物标志物,具备生物学合理性。
强化治疗和选择治疗方式的理由
在局部晚期胃癌的转化治疗场景下,化疗骨架的选择会直接影响其与免疫治疗的协同效应及临床结局。FLOT4-AIO试验显示,FLOT方案在新辅助治疗场景下可实现 31.3% 的病理完全缓解(pCR)率与65.8%的R0切除率;其亚组分析显示,FLOT联合PD-1抑制剂(纳武利尤单抗)可进一步将客观缓解率(ORR)提升至78.2%,转化切除率提升至 71.5%,但3~4级中性粒细胞减少(42.1%)与乏力(18.3%)的发生率也更高。
与之相对,聚焦SOX(替吉奥+奥沙利铂)、XELOX(卡培他滨+奥沙利铂)联合信迪利单抗(PD-1抑制剂)的国内II期试验(如CAP 02试验)报告的ORR分别为 72.3% 和 69.8%,转化切除率为 68.1% 和 65.4%。这类方案安全性更优:3-4 级胃肠道毒性(腹泻、恶心)仅为 12.5%(SOX组)和 10.8%(XELOX组),且替吉奥/卡培他滨为口服用药,可提升患者依从性,更适合老年患者或骨髓储备较差的患者。
生物标志物分层可进一步优化方案选择:KEYNOTE-859亚组分析显示,在PD-L1 CPS ≥10 的患者中,FLOT联合帕博利珠单抗可将中位总生存期(OS)延长至 18.7 个月,优于SOX联合帕博利珠单抗的 15.2 个月;而在微卫星高度不稳定(MSI-H)患者中,SOX/XELOX联合免疫治疗可实现非劣效的OS(17.9 个月vs 18.3 个月),且毒性更低。目前NCCN(2024 V1版)及CSCO(2024版)指南推荐,对于肿瘤负荷高、身体状态良好的患者,首选FLOT联合免疫治疗;合并基础疾病、耐受性有限的患者可选择SOX/XELOX联合免疫治疗。
FLOT联合纳武利尤单抗的转化治疗策略也得到了最新临床研究的验证。Guo等人开展的II期FDZL-GC001试验显示,卡瑞利珠单抗(PD-1抑制剂)联合白蛋白紫杉醇型POF方案(白蛋白紫杉醇+奥沙利铂+氟尿嘧啶),在初诊不可切除的局部晚期或寡转移胃癌患者中可实现 75.0% 的R0切除率,3 年OS率超过 62.8%。值得注意的是,研究中占比 40.4% 的腹膜后淋巴结转移患者也取得了良好结局,进一步证实了以化疗联合PD-1抑制剂为核心的方案,是转移性胃癌转化治疗的敏感、有效方案。
也有研究报道了晚期胃癌转化手术的手术结局与长期生存情况:Chen等人回顾性分析了 95 例接受全身化疗+转化手术的原发性晚期胃腺癌患者,发现晚期胃癌患者可从转化手术中获得生存获益,推荐给予足够周期的诱导化疗(通常 ≥6 周期)。Nobuhiro Nakazawa等人也报告,不可切除晚期或复发胃癌患者接受化疗联合纳武利尤单抗一线治疗后,转化手术转化率为 11.5%,转化率与良好的ECOG体力状态评分相关。
这些研究结果提示,6 个周期FLOT方案联合免疫治疗是转移性胃腺癌转化治疗的潜在优选方案。本例患者体力状态良好、无基础疾病,且手术意愿强烈,因此研究人员选择三药FLOT化疗联合纳武利尤单抗的方案,以提升R0切除率。
转化手术后,患者接近病理完全缓解(TRG1),且淋巴结阴性(0/21),但第 8、12 组肿大淋巴结无法手术切除。后续给予 54 Gy辅助放疗的目的是清除不可切除区域及高危区域的潜在转移灶。放疗可通过多重机制与手术、全身治疗发挥协同效应:化疗可诱导细胞G2/M周期阻滞,使放疗敏感性提升 1.5 倍;手术可降低原发肿瘤负荷,缩小放疗靶区体积,减少正常组织受量;免疫治疗可增强放疗诱导的免疫原性细胞死亡,促进远隔效应。
Mimura等人的研究进一步验证了放疗联合纳武利尤单抗在胃癌中的协同免疫调节效应:研究显示,大分割放疗可诱导多重免疫致敏机制:通过抗原扩散生成新发肿瘤相关抗原(TAA)特异性CD8+ T细胞,疾病未进展患者体内CD45RO+CD27+CD127+中枢记忆T细胞富集,T细胞受体β(TCRβ)库多样性得以保留以克服肿瘤异质性,同时ctDNA来源的TMB显著下降,提示肿瘤被有效清除。值得注意的是,该研究证实了该联合方案的安全性(未增加 3 级及以上不良反应),与本例患者的良好耐受情况一致。
腹膜后残留淋巴结病灶选择 54 Gy的放疗剂量,是基于循证剂量-反应关系确定的。INT 0116试验的 15 年长期随访显示,与 45 Gy剂量相比,50-54 Gy的巩固放疗可使局部复发率降低 42%,存在肉眼残留淋巴结的患者中,淋巴结清除率从 58% 提升至 76%。ASTRO/ESTRO胃癌放疗指南(2023版)明确推荐 54 Gy作为残留淋巴结病灶的标准剂量,剂量超过 54 Gy不会进一步提升局部控制率,反而会使3级及以上毒性提升 2.3 倍。
2025 年的一项meta分析(纳入 18 项研究、8923 例患者,其中 32% 的研究聚焦残留淋巴结病灶)证实,针对全身治疗后残留病灶(包括腹膜后淋巴结)的巩固放疗,可显著改善局部无复发生存期(LRFS,HR=0.63,95%CI 0.55-0.72)及OS(HR=0.77,95%CI 0.70-0.85)。亚组分析特别指出,腹膜后淋巴结受累患者属于高获益人群:LRFS改善幅度达 40%(胃周淋巴结受累患者的改善幅度为 31%)。同时,该方案潜在毒性在临床可接受范围内:27.6% 的患者出现 3 级及以上毒性,无 4 级及以上毒性报告。本例患者对治疗耐受良好,仅出现 1 级胃肠道毒性。
不过,本例患者放疗前未行PET-CT检查是局限性之一:代谢成像可识别残留代谢活性,从而指导放疗靶区划定与剂量爬坡,优化巩固放疗的患者筛选。
超高肿瘤突变负荷及适应性治疗策略的影响
本病例提出了胃癌中肿瘤突变负荷(TMB)解读的重要临床问题。尽管KEYNOTE-158研究确立的 ≥10 个突变/兆碱基的界值目前被广泛采用,但超高TMB(如 >80 个突变/兆碱基)可能代表一类独特的生物学亚型——超突变表型,这类患者对免疫治疗的应答潜力可能更强。这一现象提示,将TMB作为连续变量、而非二分类生物标志物应用可能更具临床价值:对于TMB极高的患者,或可采取更积极的免疫治疗策略;而对于应答持久的患者,也可考虑后续降阶治疗。整个诊疗过程中,基于多学科团队(MDT)的决策整合,是实现协同、根治性治疗的核心前提。通过 3 次专项MDT讨论会,团队在手术干预时机、放疗必要性、全身治疗时长等关键决策节点均达成共识。这种协作模式充分印证,整合肿瘤内科、放射肿瘤科、外科及诊断学科的专业优势,能够为复杂病例带来最大化的临床获益。
无症状后停止治疗的决定
对于免疫治疗特殊应答者,维持治疗的时长目前仍无明确界定。研究人员在患者持续达到无疾病证据(NED)状态后停止治疗的决策,是基于多学科、个体化的风险评估框架作出的,该框架纳入了以下核心因素:局部及区域病灶的根治性控制:患者接受了根治性胃切除术,同时针对不可切除的高危区域(腹膜后淋巴结)实施了辅助放疗,已实现根治性局部干预,为后续暂停全身治疗奠定了坚实基础。全身治疗的充足性与持续缓解的证据:患者完成了 2 年的规范化免疫治疗及后续维持治疗。在多年的治疗与随访期间,多次复查(包括肿瘤标志物、增强CT)均一致提示无肿瘤复发或转移征象,为确认“无病状态”提供了关键支撑。停药前复查方案与患者个体情况:研究人员原本计划在停药前通过PET-CT完成更精准的复查,但因患者个人及家庭原因暂时推迟。鉴于患者临床及影像学缓解长期稳定,经多学科团队(MDT)充分讨论后认为,暂停全身治疗并进行密切随访的获益-风险比更优。
局限性和未来方向
作为个案报告,本文研究结果仍需在更大规模的队列中得到验证。TMB在不同胃癌亚型中的预测价值有待进一步标准化,同时需要开展功能研究以明确POLD1 p.R1009H及同类意义未明变异(VUS)在驱动超突变过程中的作用。此外,尽管研究人员观察到了极为优异的治疗应答,但对于大多数转移性胃癌患者而言,免疫治疗的原发性和获得性耐药仍是重大挑战,这也凸显了深入理解肿瘤微环境内耐药机制的必要性。
展望未来,研究人员提出了寡转移性胃癌转化治疗的结构化路径:①多学科团队(MDT)评估:完善全面分期及生物标志物检测,包括二代测序(NGS)及PD-L1检测;②风险分层:对于TMB-H、MSI-H或携带POLE/POLD1突变的患者,优先选择免疫治疗;③转化治疗:根据肿瘤位置及负荷,选择化学免疫治疗±局部干预手段;④巩固治疗:对实现疾病控制的应答者给予手术和/或放疗;⑤基于应答的个体化维持治疗:根据代谢学及病理学应答情况调整治疗方案。
未来的研究应聚焦于生物标志物检测的标准化,通过实验室模型验证功能突变的作用,并整合循环肿瘤DNA(ctDNA)等动态监测工具,以指导治疗时长决策、更早发现复发。此外,针对特定人群的合理联合治疗方案(如DNA修复缺陷胃癌中免疫检查点抑制剂联合PARP抑制剂)也值得开展临床评估。
结 论
本病例充分印证了精准肿瘤免疫治疗在转移性胃癌中的潜力,证明即便是传统意义上预后极差的疾病,基于生物标志物指导的治疗方案选择也能带来前所未有的临床获益。本案例凸显了将分子检测与多学科诊疗相整合,为患者提供个体化根治性治疗的重要价值。随着肿瘤诊疗进入日益精细化的时代,这类特殊应答病例既为临床实践带来了希望,也为经分子特征筛选人群的治疗策略优化指明了方向。
参考文献:
Liu C, Li X, Qi Q, Jing F, Lv J, Qiu W and Wang S (2026) Exceptional response to chemo-immunotherapy in a patient with HER2-negative, TMB-high metastatic gastric mucinous adenocarcinoma: a case report and literature review. Front. Immunol. 16:1713214. doi: 10.3389/fimmu.2025.1713214